
¿Por qué el agua con sal no se congela? Una pregunta que muchos se hacen, pero pocos conocen, entonces, ¿Qué tan cierto es esto?
Lic. en Hidrobiología Alitzel L. Mejía A. 2024.
¿Por qué el agua con sal no se congela igual que el agua potable?
El agua con sal y el agua potable tienen propiedades fisicoquímicas diferentes, por lo que la temperatura a la que se congelan es diferente.
El agua potable se congela a una temperatura de 0°C, mientras que el agua con sal, o salada, se congela a una temperatura de -1.9°C. Considerando la salinidad del océano, que tiene 35 gramos de sal por 1000 ml de agua, que se mide en psu, unidades de salinidad práctica por sus siglas, entonces la temperatura del mar va a variar dependiendo de la sal que tenga el agua.
Composición del agua
La molécula del agua está formada por hidrógeno y oxígeno, y se representa con la unión de estos átomos que forman un ángulo de 104.5°, que se unen por enlaces covalentes, es decir, comparten electrones.
Como podrás observar en la siguiente imagen, esta configuración permite que se generen cargas parciales: una carga parcial positiva en el hidrógeno y una carga parcial negativa en el oxígeno.
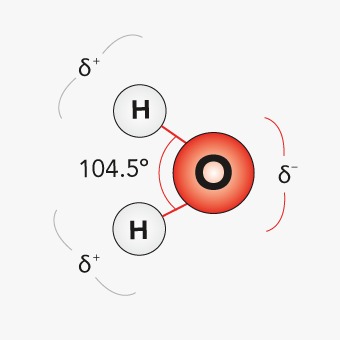
Gracias a la distribución de cargas en la molécula de agua, puede unirse fácilmente con otros átomos, esto es lo que le permite ser el mejor solvente. Esto sucede por el movimiento de electrones compartidos de los enlaces O-H, que se encuentran más tiempo con el átomo de oxígeno, que con los de hidrógeno.
¿Cómo se congela el agua?
De acuerdo con la Teoría Cinética Molecular, en los cambios de estado de la materia las moléculas poseen diferente energía cinética dependiendo del estado en el que se encuentren; es decir, en un líquido las moléculas se mueven constantemente; en un sólido se mueven de manera limitada y en el estado gaseoso tienen mucha energía cinética, por lo que se mantienen en constante movimiento.
En cuanto al agua, en estado líquido las moléculas se encuentran como en la siguiente imagen, en la que las moléculas se unen por medio de los enlaces de hidrógeno de corta duración, es decir, que cambian constantemente.
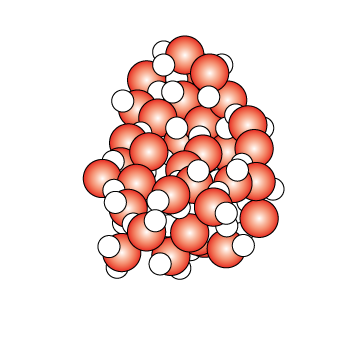
Cuando pasa del estado líquido al sólido, entre los 0° C y 4 °C, se empiezan a formar redes que forman estructuras hexagonales, como las que se observan en la siguiente imagen, en la cual los enlaces tienen mayor duración.
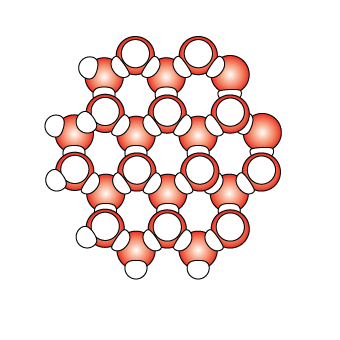
¿Por qué se congela a diferente temperatura el agua con sal?
Como mencionamos anteriormente, las propiedades fisicoquímicas del agua con sal cambian, normalmente el agua se enlaza al hidrógeno con el oxígeno, pero en este caso, la sal hace más difícil este proceso, porque la sal (NaCl) se separa en sus iones sodio (Na +) y cloro (Cl–) al disolverse en el agua; mientras que los iones del cloruro se unen al hidrógeno y los iones del sodio se unen al oxígeno, pero sin formar un enlace, sino que lo rodean con sus cargas. A esto se le llama capa de hidratación, como se observa en la siguiente imagen.
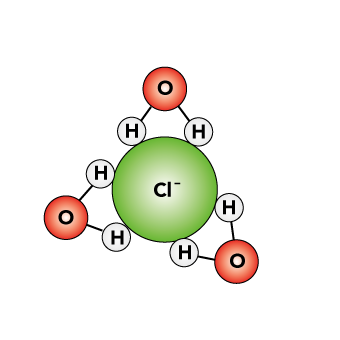
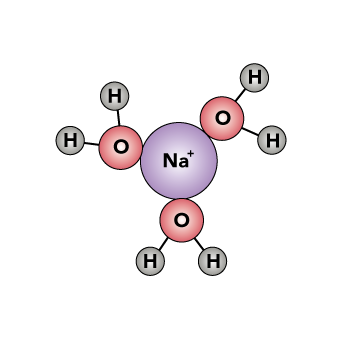
Figura 4. Representación de la disolución de sal en agua, en Avissar, Y. et al., 2018, OpenStax. CC BY 3.0.
Además, las partículas de sal reemplazan a las partículas de agua; en consecuencia, la estructura que se forma es muy semejante a la siguiente figura, en la que se representa la solución de 2 moléculas de agua y 1 molécula de sal, ocasionando que la tasa de congelamiento baje.
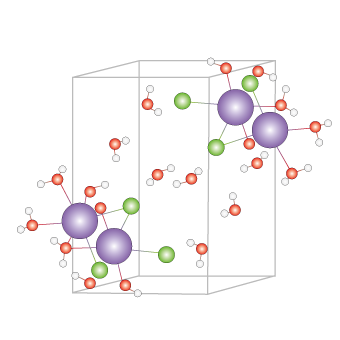
Entonces, mientras el agua tenga más sal, menor será la temperatura de congelamiento, es decir, que estará más cerca de los -2ºC, por lo que tardará más tiempo en congelarse; y, por el contrario, si tiene poca sal, la temperatura de congelamiento será mayor, o sea que estará más cerca de los 0º en la escala de Celsius, por tanto, se congelará más rápido.
Revisa nuestros servicios: limpieza de cisternas y tinacos en el Valle de México.
Usos del agua salada
Gracias a que la sal retarda el descongelamiento, como ya dijimos, por sus propiedades fisicoquímicas, se puede aprovechar esta propiedad para manejar algunos alimentos; por ejemplo, podemos agregar sal a los hielos para que nos duren más, lo que es de gran utilidad para los heladeros, desde que hacen los helados hasta para conservarlos fríos. Pero también tiene usos comunes, por ejemplo, si quieres que tus refrescos permanezcan bien fríos durante un picnic, agrega un poco de sal a tus hielos, evitará que se derritan rápidamente.
Si deseas lavar tu cisterna o tinaco con expertos en limpieza ¡Contáctanos! Cotiza ahora tu servicio, sin costo alguno.
Referencias
Avissar, Y., Choi, J., DeSaix, J. et al. (2018), Representación de la disolución de sal en agua [imagen]. En Biology. Recuperado de: https://openstax.org/books/biology/pages/preface
Avissar, Y., Choi, J., DeSaix, J. et al. (2018), Molécula de agua [imagen]. En Biology. Recuperado de: https://openstax.org/books/biology/pages/preface
Baptiste Journaux/University of Washington. (2021), Estructuras cristalinas de hidratos de sal [imagen]. En ScienceAlert. Recuperado de: https://www.sciencealert.com/discovery-of-two-new-forms-of-salt-water-could-rewrite-fundamental-chemistry
CK-12 Foundation. (2022). Disposición molecular de agua congelada [imagen]. En LibreTexts. Recuperado de: https://espanol.libretexts.org/Quimica/Qu%C3%ADmica_Introductoria%2C_Conceptual_y_GOB/Qu%C3%ADmica_Introductoria_(CK-12)/15%3A_Agua/15.02%3A_Estructura_de_Hielo
CK-12 Foundation. (2022). Disposición molecular de agua líquida [imagen]. En LibreTexts. Recuperado de: https://espanol.libretexts.org/Quimica/Qu%C3%ADmica_Introductoria%2C_Conceptual_y_GOB/Qu%C3%ADmica_Introductoria_(CK-12)/15%3A_Agua/15.02%3A_Estructura_de_Hielo
MEDCLIC (s.f) El agua de Mar.





Dejar un comentario